У человека более ста миллиардов нейронов. Каждый нейрон состоит из тела и отростков — обычно одного длинного аксона и нескольких коротких разветвлённых дендритов. Благодаря этим отросткам нейроны контактируют друг с другом и образуют сети и круги, по которым циркулируют нервные импульсы. На протяжении всей жизни мозг человека теряет нейроны. Такая гибель клеток генетически запрограммирована, но в отличие от клеток других тканей нейроны не способны делиться. В этом случае действует иной механизм: функции погибших нервных клеток берут на себя их «коллеги», которые увеличиваются в размерах и формируют новые связи, компенсируя бездействие погибшей клетки.
Согласно расхожему мнению, нервные клетки не восстанавливаются. Однако это не соответствует действительности: нейроны — клетки нервной системы — действительно, не могут делиться, как клетки других тканей, но они возникают и развиваются даже в мозге взрослого человека. К тому же нейроны способны восстанавливать утраченные отростки и контакты с другими клетками.
Нервная система человека состоит из центральной части и периферической. Центральная включает в себя головной и спинной мозг. В головном мозге находится самое обширное скопление нейронов. От тела каждого отходят многочисленные отростки, которые формируют контакты с соседними нейронами. Периферическую часть образуют спинномозговые, вегетативные и черепные узлы, нервы и нервные окончания, обеспечивающие проведение нервных импульсов к конечностям, внутренним органам и тканям. В здоровом состоянии нервная система — слаженный механизм, если одно из звеньев сложной цепи не выполняет свои функции, страдает всё тело. К ускоренной гибели нейронов приводят, к примеру, тяжёлые поражения головного мозга после инсультов, болезнь Паркинсона, болезнь Альцгеймера. На протяжении нескольких десятилетий учёные пытаются понять, возможно ли стимулировать восстановление утраченных нервных клеток.
И всё-таки они регенерируют
Первые научные публикации, подтверждающие рождение новых нейронов в мозге взрослых млекопитающих, принадлежат американскому исследователю Джозефу Олтману (Joseph Altman). В 1962 году в журнале Science вышла его статья «Формируются ли новые нейроны в мозге взрослых млекопитающих?», в которой Олтман рассказывал о результатах своего эксперимента. С помощью электрического тока он разрушил одну из структур мозга крысы (латеральное коленчатое тело) и ввёл туда радиоактивное вещество, которое проникает в новые клетки. Через несколько месяцев Олтман обнаружил новые радиоактивные нейроны в таламусе и коре головного мозга. В последующие годы Олтман опубликовал ещё несколько работ, доказывающих существование нейрогенеза в мозге. К примеру, в 1965-м была опубликована его статья в журнале Nature. Несмотря на это в научном сообществе у Олтмана было много оппонентов, только спустя несколько десятилетий, в 1990-х, его работы получили признание, а феномен рождения новых нейронов — нейрогенез — стал одной из самых увлекательных областей нейрофизиологии.
Сегодня уже известно, что нейроны могут зарождаться в мозге взрослого млекопитающего из так называемых нейрональных стволовых клеток. Пока установлено, что происходит это в трёх областях головного мозга: зубчатой извилине гиппокампа, субвентрикулярной области (в боковых стенках латеральных желудочков мозга) и коре мозжечка. В мозжечке нейрогенез протекает наиболее активно. Эта область мозга отвечает за приобретение и сохранение информации о бессознательных автоматизированных навыках — к примеру, разучивая танец, мы постепенно перестаём задумываться о движениях, выполняем их автоматически; информация об этих па хранится именно в мозжечке. Пожалуй, самым интригующим для исследователей остаётся нейрогенез в зубчатой извилине. Именно здесь рождаются наши эмоции, хранится и обрабатывается пространственная информация. Пока не удаётся разобраться, каким образом вновь образованные нейроны воздействуют на уже сформированные воспоминания и взаимодействуют со зрелыми клетками этого отдела мозга.
Опыты с крысами в лабиринтах различных конструкций помогают учёным понять, что происходит с новыми нейронами в мозге и как они встраиваются в отлаженную работу уже существующих клеток нервной системы.
Лабиринт на память
Для того чтобы понять, как новые нейроны взаимодействуют со старыми, активно изучают процесс обучения животных в водном лабиринте Морриса. В ходе опыта животное помещают в бассейн 1,2–1,5 м в диаметре, глубиной 60 см. Стены бассейна различны, при этом в определённом месте бассейна в нескольких миллиметрах под водой скрыта платформа. Погружённая в воду лабораторная крыса стремится быстрее ощутить твёрдую почву под ногами. Плавая в бассейне, животное узнаёт, где находится платформа, и в следующий раз находит её уже быстрее.
С помощью обучения крыс в водном лабиринте Морриса удалось доказать, что формирование пространственной памяти приводит к гибели самых молодых нейронов, но активно поддерживает выживание клеток, которые образовались примерно за неделю до опыта, то есть в процессе формирования памяти происходит регулирование объёма новых нейронов. В то же время появление новых нейронов обеспечивает возможность формирования новых воспоминаний. В противном случае животные и человек не могли бы адаптироваться к меняющимся условиям внешней среды.
Было отмечено, что столкновение со знакомыми предметами активирует различные группы нейронов гиппокампа. По-видимому, каждая группа таких нейронов несёт воспоминание о конкретном событии или месте. Причём жизнь в разнообразной среде стимулирует нейрогенез в гиппокампе: мыши, которые проживают в клетках с игрушками и лабиринтами, имеют больше вновь образованных нейронов в гиппокампе, чем их сородичи из стандартных пустых клеток.
Примечательно, что нейрогенез активно проходит только в тех зонах мозга, которые непосредственно отвечают за физическое выживание: ориентацию по запаху, ориентацию в пространстве, за формирование двигательной памяти. Обучение абстрактному мышлению активно проходит в молодом возрасте, когда мозг ещё растёт и нейрогенез затрагивает все зоны. А вот после достижения зрелости мыслительные функции развиваются за счёт перестройки контактов между нейронами, но не за счёт появления новых клеток.
Несмотря на несколько неудачных попыток, поиски неизвестных ранее очагов нейрогенеза во взрослом мозге продолжаются. Это направление считается актуальным не только для фундаментальной науки, но и для прикладных исследований. Многие заболевания центральной нервной системы связаны с потерей определённой группы нейронов мозга. Если бы можно было вырастить им замену, то болезнь Паркинсона, многие проявления болезни Альцгеймера, негативные последствия эпилепсии или инсульта были бы побеждены.
Заплатки для мозга
Ещё один любопытный метод, взятый на вооружение нейробиологами в их исследованиях, — вживление эмбриональных стволовых клеток в мозг взрослого животного для восстановления утраченных функций. Пока подобные эксперименты приводят к отторжению привнесённой ткани или клеток из-за сильного иммунного ответа, но если стволовые клетки и приживаются в некоторых случаях, они перерастают в клетки глии (сопровождающей ткани), а вовсе не в нейроны. Даже если в будущем нейрогенез можно будет активировать в любой зоне мозга, неясно, каким образом вновь образованные нейроны будут формировать связи внутри уже сложившейся сети нервных клеток и будут ли они вообще на это способны. Если гиппокамп к такому процессу готов, то появление новых нейронов в других областях мозга может нарушить те сети, которые устанавливались годами; вместо ожидаемой пользы, возможно, будет нанесён лишь вред. Тем не менее учёные продолжают активно изучать возможности нейрогенеза в других участках мозга.
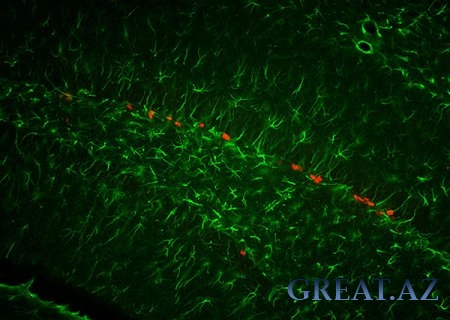
На рисунке показан процесс образования новых нейронов в гиппокампе взрослого млекопитающего при облучении малыми дозами радиации. Новые нейроны красные, глия — зелёная.
Совсем недавно, в феврале 2010-го, группа канадских исследователей из университета Торонто (University of Toronto) и университета Ватерлоо (University of Waterloo) опубликовала результаты экспериментов с использованием циклоспорина А в качестве стимулятора нейрогенеза. В культуре клеток была показана способность циклоспорина А увеличивать рост и количество клеток в колонии, а введение этого вещества взрослым мышам привело к увеличению нейрональных стволовых клеток в мозге.
Наряду с искусственными веществами, исследуют и свойства эндогенных молекул, которые способны усилить нейрогенез. Наибольшее внимание здесь заслуживают нейротрофические факторы, которые вырабатываются организмом животных. Это фактор роста нервов (NGF), нейротрофический фактор головного мозга (BDNF), нейротрофины-1, -3 и -4.
Нейротрофические факторы принадлежат к группе белков, которые поддерживают рост, развитие и выживаемость нервных клеток. Если доставить нейротрофический фактор в повреждённую область мозга, то можно значительно замедлить гибель нейронов, поддержать их жизнедеятельность. Хотя нейротрофические факторы не в состоянии активировать появление новых нервных клеток в головном мозге, они обладают уникальным свойством — активируют восстановление отростков нервных клеток (аксонов) после повреждения или утраты. Длина некоторых аксонов достигает метра, и именно аксоны проводят нервные импульсы из головного мозга к нашим конечностям, внутренним органам и тканям. Целостность этих путей нарушается при переломах позвоночника и смещении позвонков. Регенерация аксонов — это надежда на восстановление способности двигать руками и ногами в таких случаях.
Ростки и отростки
Первые работы, доказывающие возможность регенерации аксонов, были опубликованы в 1981 году. Тогда появилась статья в журнале Science, которая доказывала, что такая регенерация возможна. Обычно регенерации аксонов мешают несколько причин, но если препятствие устранить, то аксоны активно прорастают и создают новые контакты вместо утраченных. С началом изучения регенерации аксонов была открыта новая эра в медицине, теперь у людей с повреждением спинного мозга появилась надежда, что двигательные способности можно вернуть. Эти исследования получили широкую поддержку, причём не только различных исследовательских центров. Так, известный актёр Кристофер Рив, сыгравший главную роль в фильме «Супермен» и ставший инвалидом после перелома позвоночника, основал вместе со своей женой фонд для поддержки подобных исследований — Christopher and Dana Reeve Paralysis Foundation.

Последние исследования нейробиологов дают некоторые надежды инвалидам, прикованным к коляске из-за повреждений нервной системы.
Главная преграда на пути регенерации аксонов — это формирование рубцовой ткани, которая отгораживает повреждения спинного мозга или периферических нервов от окружающих клеток. Считается, что такой рубец спасает близлежащие области от возможного проникновения токсинов из поврежденной зоны. В результате аксоны не могут пробиться сквозь рубец. Показано, что основу рубцовой ткани составляют протеингликаны (хондроитинсульфат).
Исследования, проведённые в 1998 году в лаборатории профессора Дэвида Муира (David Muir) в Институте мозга при университете Флориды, показали, что возможно разрушить протеингликаны с помощью бактериального фермента хондроитиназы АВС. Но даже при удалении механического препятствия рост аксонов всё ещё замедлен. Дело в том, что в месте повреждения присутствуют мешающие регенерации вещества, такие как MAG, OMgp, Nogo. Если их заблокировать, то можно добиться значительного усиления регенерации.
Наконец, для успешного роста аксонов важно поддерживать высокий уровень нейротрофических факторов. Несмотря на то, что нейротрофины оказывают позитивный эффект на регенерацию нервной системы, клинические испытания выявили значительные побочные эффекты, такие как потеря веса, аппетита, тошнота, появление психологических проблем. Чтобы усилить регенерацию, в место повреждения можно было бы ввести стволовые клетки, но существуют данные о том, что вживление стволовых клеток в спинной мозг может спровоцировать появление опухолей.
Даже если аксон вырос и стал способен проводить нервные импульсы, это ещё не означает, что конечности начнут нормально функционировать. Чтобы это произошло, необходимо наличие множества контактов (синапсов) между аксонами нервных клеток и мышечными волокнами, которые и приводят в движение тело человека. Восстановление таких контактов занимает длительное время. Конечно, выздоровление можно ускорить, если выполнять специальные физические упражнения, но за несколько месяцев или даже лет невозможно полностью воссоздать картину нервных контактов, которая формировалась десятилетия, с самого первого дня зарождения человеческой жизни. Число таких контактов не поддаётся подсчету, вероятно, оно сравнимо с числом звёзд во Вселенной.
Но есть и положительный момент — всё-таки за последние годы удалось сдвинуться с мёртвой точки, теперь хотя бы понятно, какими способами можно пытаться ускорить нейрорегенерацию.